بحث عن المعادلة الكيميائية الحرارية جاهز doc
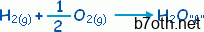
المعادلات الكيميائية الحرارية
أول مسعر ثلجي في العالم، اُستخدم في شتاء 1782-83، من قِبل أنطوان لاڤوازييه و پيير-سيمون لاپلاس، لتحديد الحرارة المتحولة في مختلف التغيرات الكيميائية؛ الحسابات كانت مبنية على اكتشاف جوسف بلاك السابق للحرارة الكامنة. هذه التجارب تعد بداية الكيمياء الحرارية.
الكيمياء الحرارية thermochemistry هي دراسة الأفعال الحرارية المرافقة للتفاعلات الكيمياوية. بعض التفاعلات ناشر للحرارة exothermic، مثل احتراق الفحم في الهواء إذ ترتفع درجة حرارته نتيجة للتفاعل الشكل (1)، في حين يكون بعضه الآخر ماصاً للحرارة endothermic كتفاعل الفحم المتوهج مع بخار الماء الشكل (2). وفي حالات نادرة يكون الفعل الحراري معدوماً تماماً كما في تفاعل الكحول مع حمض الخل لتشكيل الإستر.
تقتضي الدراسة الكمية للفعل الحراري تعريفاً دقيقاً لما يُسمى حرارة تفاعل عند الدرجةt : هي كمية الحرارة، مقدرة بالجول، المنتشرة أو الممتصة في أثناء التفاعل، أي المتبادلة من قبل المواد المتفاعلة والنواتج مع الوسط الخارجي بعد أن تعود هذه المواد كلها إلى الدرجة t التي بدأ بها التفاعل. واصطُلح على اعتبار كمية الحرارة مقداراً جبرياً سالباً للتفاعلات الناشرة للحرارة وموجباً للتفاعلات الماصة للحرارة. الكيمياء الحرارية في الديناميكا الحرارية وفي الكيمياء الطبيعية هي دراسة تولد الحرارة أو امتصاصها في التفاعلات الكيميائية. وتهتم عامة بتبادل الحرارة المرافق للتحولات، مثل الاختلاط وتحول الحالة والتفاعلات الكيميائية وما إلى ذلك، وتشمل حسابات هذه الكميات من حيث سعة الحرارة وحرارة الاحتراق وحرارة التشكيل. تعتمد قوانين الكيمياء الحرارية على قانونين:
قانون لاڤوازييه ولاپلاس (1782): تبادل الحرارة المصاحب للتحول يساوي عكس تبادل الحرارة المصاحب للتحول في الجهة المعاكسة.
قانون هس (1840): تبادل الحرارة المصاحب للتحول هو نفسه إذا ما حدث في عملية واحدة أو في عدة خطوات
سبق كلا القانونين أول قانون للديناميكا الحرارية (1850) لكنهما نتيجة مباشرة له.
حرارتا التفاعل
إن تطبيق المبدأ الأول في الترموديناميك[ر: التحريك الحراري] على التفاعلات يؤدي إلى قانون هس Hess الذي ينص على أن: الحرارة المرافقة لتفاعل ما لا تتعلق إلا بالحالتين الابتدائية والنهائية، وهي مستقلة عن الطريق المسلوك (عدد المراحل وطبيعتها مثلاً) على أن يتم التفاعل إما عند ضغط ثابت أو حجم ثابت.
تتوافق التفاعلات عملياً مع أحد هذين الشرطين، فهي تتم في حجم ثابت إذا أجريت في مفاعل مغلق كمحرك الاحتراق الداخلي، أو إذا كان حجم النواتج مماثلاً لحجم المواد المتفاعلة (جميع المواد الصلبة أو السائلة لها كتل حجمية متقاربة، أو في حالة الغازات إذا كان عدد المولات الداخلة في التفاعل مساوياً لعدد مولات النواتج). أما جميع التفاعلات التي تتم تحت الضغط الجوي فهي تفاعلات تتم تحت ضغط ثابت.
للتمييز بين هاتين الحالتين يمكن الانطلاق من تغير الطاقة الداخلية ΔU لجملة المواد المتفاعلة الذي يُعطى في أثناء التفاعل بالعلاقة: ΔU=W + Q
حيث Q وW: الحرارة والعمل المتبادلان مع الوسط الخارجي، ويكون العمل غالباً ناجماً عن قوى الضغط: W = – P. ΔV وبهذا يكون لكمية الحرارة شكلان للقياس:
1ـ الحجم ثابت: أي إن عمل قوى الضغط معدوم، وحرارة التفاعل بحجم ثابت Qv مساوية لتغير الطاقة الداخلية للجملة: Qv= ΔU.
2ـ الضغط ثابت: في هذه الحالة يرتبط تغير الحرارة Qp بتغير الأنطلبية[ر]:
Qp =ΔU – W= ΔU + P. ΔV ونظراً لثبات الضغط: Qp =ΔU + Δ (P.V)
وبالتالي Qp =ΔH، أي إن كمية حرارة التفاعل تحت ضغط ثابت تساوي تغير أنطلبية الجملة.
اتختلف حرارتا التفاعل السابقتان عموماً إلا إذا اشتركت في التفاعل غازات، وترتبطان عندئذ ببعضهما، في حالة الغازات الكاملة، بالعلاقة: Qp = Qv+ (n2-n1).RT
حيث n1 وn2 عدد مولات الغازات المتفاعلة والناتجة على الترتيب.
يجب الانتباه إلى عدد من الاصطلاحات عند كتابة حرارة تفاعل:
1 – توافِق حرارة التفاعل كمية محددة من المواد المتفاعلة أو المنتَجة، هذه الكمية تظهر في معادلة التفاعل، أي إن مضاعفة أمثال المعادلة يقتضي مضاعفة الحرارة المرافقة أيضاً. وفي حالة تشكل مركّب بدءاً من عناصره تؤخذ أنطلبية التشكل العيارية مول واحد من المركب، والمقصود بعيارية أن القياس تم بالدرجة k298K وبالضغط b1 bar وبالشكل الفيزيائي الأكثر استقراراً للمواد المتفاعلة في هذه الشروط. تعد المراجع القديمة الضغط العياري مساوياً للضغط الجوي (b1.018 bar)، وقد تغير هذا الشرط حديثاً إلى القيمة 1 bar.
2 – بحالة تفاعل عكوس تُكتب القيمة الموافقة للاتجاه المباشر.
3 – يجب تحديد الحالة الفيزيائية لكل مادة في التفاعل، صلبة أم سائلة أم غازية.
4 – إذا لم تُذكر درجة الحرارة التي يتم عندها التفاعل عُدّت مساوية لـِ k298K، والمقصود بذلك أن المواد المتفاعلة أُخذت في هذه الدرجة كما النواتج النهائية. أما في أثناء التفاعل فيمكن أن تتغير درجة حرارة الجملة في أي اتجاه.
المعادلة الكيميائية الحرارية
هي معادلة كيميائية موزونة مع تحديد التغير في المحتوى الحراري مقاساً بالكيلوجول .
مثال :
| النظامية للتفاعل = ـ 250.1 كيلوجول . | DHْهْ |
إذن التفاعل طارد للحرارة .
عند كتابة معادلة كيميائية حرارية نراعي ما يلي :
1- عدد المولات في المعادلة والتي تشير إليها أرقام التوازن .
2- كتابة حالة المادة في التفاعل لأن المحتوى الحراري للمادة تابع لحالتها .
مثال :
| ْH Dه= ـ 285.3 كيلوجول . |
| ْH Dه= ـ 241.8 كيلوجول . |
3- حيث أن المحتوى الحراري تابع لدرجة الحرارة فيجب ذكرها في المعادلة , إذا كانت غير الدرجة المتفق عليها وهي 25 ْ م ( حوالي 298 ْ مطلقة أو كلفن ).
4- عند كتابة المعادلة الكيميائية الحرارية يمكن وضع كمية الحرارة مع المواد المتفاعلة أو الناتجة ، ولكن العلماء اتفقوا على أن يكتب المحتوى الحراري بقرب المعادلة وبشكل مستقل .
| مثال (1) : |
التفاعل طارد للحرارة فالحرارة هي أحد النواتج .
هذه طريقة مقبولة ولكن الاتفاق هو :
ْH Dه= ـ 726 كيلوجول ( التفاعل طارد للحرارة والإشارة السالبة تشير إلى ذلك ).
| مثال (2) : |
التفاعل ماص للحرارة فالحرارة هي أحد المتفاعلات .
ْH Dه= + 227 كيلوجول كيلو جول والإشارة ( + ) تشير إلى أن التفاعل ماص للحرارة .
.
.
.
__________________________________
اضغط الرابط أدناه لتحميل البحث كامل ومنسق جاهز للطباعة


